Erstmals haben Mediziner einem blinden Patienten mit einer optogenetischen Therapie das Sehen ermöglicht. Für diesen Machbarkeitsnachweis behandelte das internationale Team einen 58-jährigen Mann, der durch die Netzhauterkrankung Retinitis pigmentosa seit Jahrzehnten blind war.
Nach der Gentherapie konnte der Patient mithilfe einer Spezialbrille im Labor Gegenstände erkennen und greifen (siehe Video unten). Im Alltag registrierte er etwa ein Telefon, eine Tür oder einen Zebrastreifen, wie das Team um José-Alain Sahel von der University of Pittsburgh School of Medicine und Botond Roska von der Universität Basel im Fachblatt "Nature Medicine" schreibt.
Experten bewerten die Studie einhellig als Durchbruch
"Zum ersten Mal hat eine therapeutische Intervention, die auf Optogenetik beruht, eine Art des Sehens ermöglicht", sagt Stylianos Michalakis von der Ludwig-Maximilians-Universität München (LMU), der nicht an der Arbeit beteiligt war. "Das ist eine Mauer, die erstmals durchbrochen wurde." Bei Retinitis pigmentosa käme eine solche Therapie, falls sie eines Tages zugelassen wird, jedoch nur für Patienten im Spätstadium infrage, betont der Leiter der Arbeitsgruppe "Gentherapie von Augenerkrankungen".
Retinitis pigmentosa (RP) umfasst eine Gruppe von Erkrankungen, bei denen durch verschiedene Erbgut-Mutationen die Lichtrezeptoren der Netzhaut - der Retina - zugrunde gehen. Bislang sind mehr als 70 Gene bekannt, bei denen Mutationen die Krankheit verursachen können. Weltweit sind den Forschern zufolge etwa zwei Millionen Menschen betroffen, in Deutschland schätzt Michalakis die Zahl auf bis zu 40.000.
Bei der fortschreitenden Erkrankung degenerieren die Lichtrezeptoren in der oberen Schicht der Netzhaut und sterben schließlich ab - die Patienten erblinden. Als einzige kurative Behandlung ist in Europa seit 2018 eine Gentherapie mit dem Mittel Luxturna zugelassen. Die über 800.000 Euro teure Behandlung hilft jedoch nur Menschen mit Mutationen des Gens RPE65, die die Erkrankung im Frühstadium haben - also wenn die Lichtrezeptorzellen noch nicht abgestorben sind. Das betrifft nach Angaben von Michalakis weniger als ein Prozent der RP-Patienten. Sie bekommen einmalig virale Vektoren ins Auge injiziert, die funktionsfähige Kopien des defekten Gens in diese Zellen tragen sollen.
Der nun vorgestellte Ansatz ist dagegen mutationsübergreifend. Er soll jenen Patienten, die bereits erblindet sind, wieder ein zumindest rudimentäres Sehen ermöglichen. In der Studie, die zunächst Sicherheit und Wirksamkeit des Ansatzes prüfen sollte, wollten die Forscher das Verfahren eigentlich an 15 Menschen testen. Wegen der Corona-Pandemie beendete jedoch vorerst nur der 58-jährige Franzose die Untersuchung.

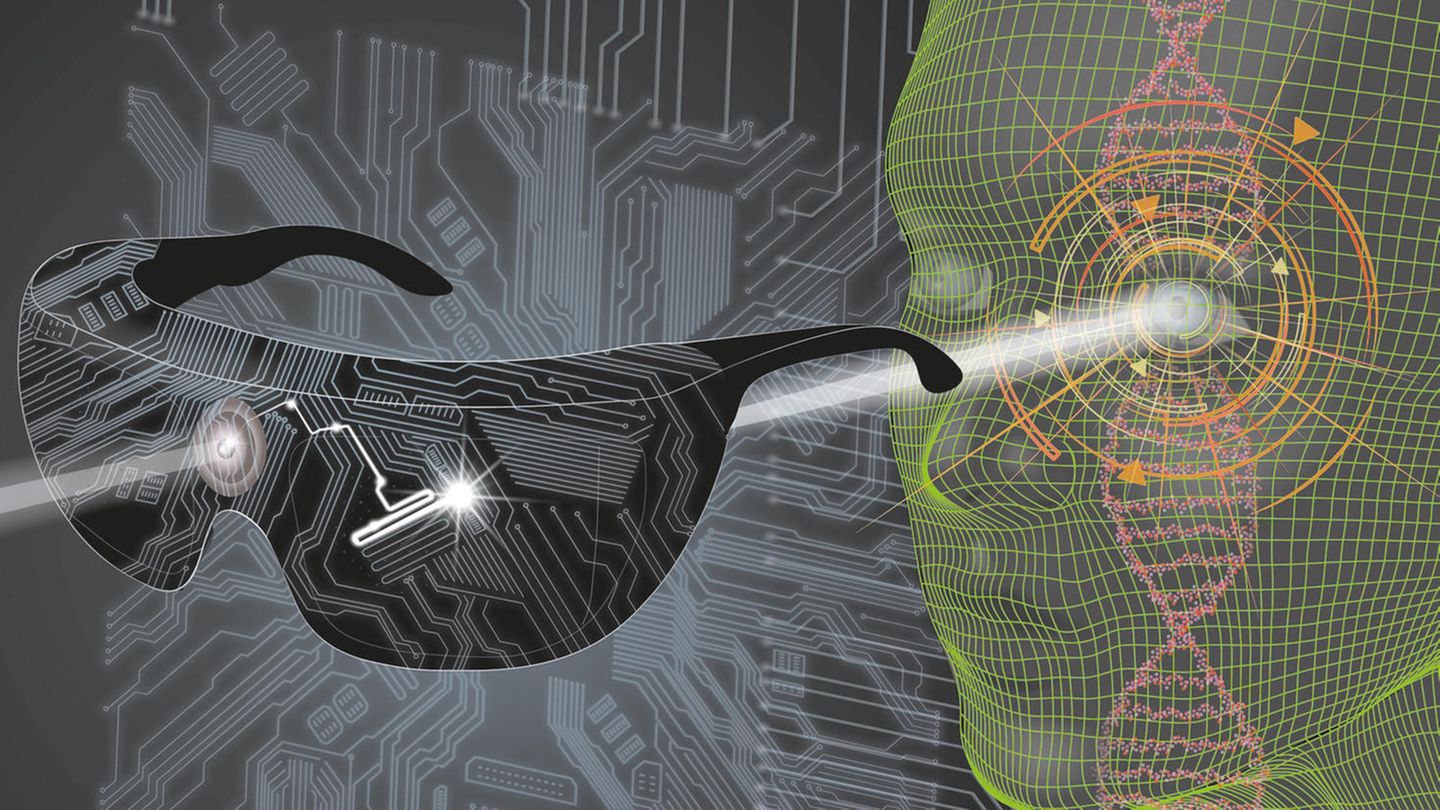
Bei der Optogenetik geht es grundsätzlich darum, genetische Informationen für bestimmte, durch Licht aktivierbare Funktionen in Zielzellen zu schleusen. In der Studie injizierte das Team in das schwerer betroffene Auge des Mannes einmalig Viren, die den Bauplan für ein lichtempfindliches Protein trugen. Dieses aus Mikroalgen stammende Protein - ein sogenanntes Kanalrhodopsin namens ChrimsonR - bildet in bestimmten Zellen der unteren Netzhaut einen Ionenkanal. Damit erzeugen die Zellen aus einfallendem Licht elektrische Signale, die sie an das Sehzentrum im Gehirn weiterleiten.
Dieser Ionenkanal reagiert besonders sensibel auf Licht mit einer Wellenlänge von 590 Nanometern, was einem gelblichen Orange entspricht. Allerdings reicht Tageslicht zu seiner Aktivierung bei weitem nicht aus. Daher entwickelte das Team eine Kamerabrille, die die Bilder der Umgebung in Echtzeit auf genau dieser Wellenlänge mit sehr hoher Intensität durch die Pupille auf die Netzhaut projiziert.
Der Patient begann das Training mit der Brille viereinhalb Monate nach der Injektion - etwa so lange brauchen die Zielzellen in der unteren Netzhaut, um die Ionenkanäle zu bilden. Sieben Monate nach Aufnahme des Trainings berichtete der Mann von visuellen Eindrücken, allerdings nur, wenn er die Spezialbrille trug. In verschiedenen Tests konnte er damit Gegenstände, die vor ihm auf einem weißen Tisch lagen, recht zuverlässig erkennen und greifen. Auch konnte er etwa auf einem Zebrastreifen die Zahl der Streifen zählen.
Im Video: Aufnahmen aus der Versuchs-Reihe mit einem blinden Patienten
Die Besserung betraf nur das behandelte Auge. Messungen per Elektroenzephalografie (EEG) bestätigten Aktivitäten im Sehzentrum der Großhirnrinde (Kortex). In einem Versuch stellten die Forscher auf den Tisch vor dem Patienten entweder einen Becher oder aber sie ließen den Tisch leer. Allein aus der Aktivität des Sehzentrums ließ sich mit knapp 80-prozentiger Wahrscheinlichkeit ableiten, ob der Becher auf dem Tisch stand oder nicht. Das werten die Forscher als Bestätigung dafür, dass die neuronale Aktivität mit dem Gegenstand zusammenhing.
Beim Sehen bewegte der Patient den Kopf hin und her, um seine Umgebung "abzuscannen". Die Autoren erklären das damit, dass sein Blickfeld einem Winkel von nur etwa 8,2 Grad entspricht - das ist ein Bruchteil dessen, was ein normal Sehender erfasst.
Im Untersuchungszeitraum von 84 Wochen fanden die Forscher keinerlei Hinweise auf schädliche Auswirkungen: So gab es etwa keine Belege dafür, dass die extrem intensiven Lichtimpulse die Netzhaut schädigten. Zudem stellte das Team keine Zeichen von Entzündungsreaktionen fest.
Die Autoren warnen jedoch vor überzogenen Hoffnungen. Derzeit sei nicht zu erwarten, dass Patienten nach einer solchen Therapie etwa Gesichter erkennen oder gar lesen könnten, betonten sie auf einer eigens anberaumten Pressekonferenz. Dennoch ermögliche das Verfahren eine deutliche Steigerung der Lebensqualität - zumal der 58-Jährige nur mit einer niedrigen Dosis behandelt worden sei.
Weitere Studien sollen in den nächsten Jahren folgen
Auf die Frage, wann dieser Ansatz mehr Patienten zur Verfügung stehe, antwortete Sahel, zunächst seien weitere Studien mit mehr Teilnehmern nötig: "Es ist schwierig vorherzusagen, wie viel Zeit das erfordert." Möglicherweise könne der Ansatz innerhalb von fünf Jahren mehr Menschen angeboten werden, doch zunächst müsse seine Sicherheit abgeklärt werden. Mehrere der Autoren arbeiten für das französische Unternehmen Gensight Biologics, das die Studie mitfinanziert hat.
Peter Hegemann von der Humboldt-Universität Berlin spricht von einem "Durchbruch in eine neue Ära zur Behandlung von Retinitis pigmentosa". Der klinische Einsatz sei jedoch "noch lange nicht absehbar und vieles kann in naher Zukunft verbessert werden", betont der Neurowissenschaftler, der zu den Entdeckern der Kanalrhodopsine zählt.
Michael Schmid von der Schweizer Universität Freiburg (Fribourg) hält die Arbeit für "einen sehr bedeutenden Schritt auf dem langen und schwierigen Weg, eine visuelle Prothese zu entwickeln". "Die Weiterentwicklung der Optogenetik für den Menschen ist nicht nur für die Behandlung der Blindheit, sondern auch generell für die Therapie neurologischer Erkrankungen ein exzellenter Fortschritt", betont er.
Der LMU-Experte Michalakis hält in der Zukunft eine Anwendung unter anderem bei anderen degenerativen Netzhauterkrankungen für vorstellbar - etwa im Spätstadium der Altersbedingten Makuladegeneration (AMD) oder der Diabetischen Retinopathie.
Eine Schwäche des vorgestellten Ansatzes sei noch, dass das in der Studie verwendete Kanalrhodopsin ChrimsonR für seine Aktivierung sehr intensive Lichtimpulse benötige, weshalb die Spezialbrille erforderlich sei. Um darauf verzichten zu können, brauche man ein wesentlich lichtempfindlicheres Kanalrhodopsin.
Das gibt es möglicherweise bereits, wie der Optogenetik-Pionier Zuho-Hua Pan von der Wayne State University School of Medicine in Detroit betont: Er habe an seinem Institut ein einsatzfähiges lichtempfindlicheres Kanalrhodopsin entwickelt, das bei Mäusen die erforderliche Lichtintensität deutlich reduziere. "Wenn sich dies auf den Menschen übertragen ließe, bräuchten die behandelten Patienten bei den meisten normal vorkommenden Lichtverhältnissen keine Brille mehr zu tragen", schreibt Pan in einer Stellungnahme zu der Studie.